≪TNM分類(UICC)の番外転移:腹膜播種、直腸転移、吻合膀胱頸口≫
TNM分類に無い疑転移で、PSA再発を来たしたサルベージでは放射線の局処床(prostatic bed)照射で約半数に顕著な臨床的効果を認め、各機関で実施しているスタディに於いても5年PSA非再発率は70%程度とのデータがある。何故であろうか?
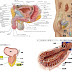
前立腺がんでの転移の多くは血行性による経骨からで、経路的に膀胱転移するリンパ行性は稀である。腹膜播種や直腸などへの転移はあまり聴かない。その理由は直腸と前立腺の間隙に極めて透過性の悪いデノビエ筋膜(膀胱直腸間膜)が腹膜から分岐されていて、癌細胞の接着や浸潤は物理的に容易ではない。腹膜播種のある胃や卵巣の癌は腹腔内にあり、膀胱、前立腺そして子宮などアウトポ-トは骨盤内にあって腹膜で腹腔とアイソレートされている。前立腺周囲は膀胱から連続して膀胱筋膜に覆われていて、癌細胞は腹膜骨盤腔側への浸潤播種を困難とされる。(下図参照)
 |
| 前立腺Bモード |
 |
| 前立腺ー直腸デノビエ筋膜 |
膀胱頸部に癌は、或いは前立腺(基底細胞、神経内分泌細胞、腺房細胞)は残るのだろうか?RRPは精嚢、前立腺、神経束、内膀胱括約筋(自律神経:不随意)及び所属リンパ節を切除するが、外尿道括約筋(随意性)は残している。(下図の黒線枠内)
膀胱吻合部或いは局処巣床に放射線をアテズッポにでも照射することで約半数の人に顕著な効果があると云われている。PSA低下があるならば前立腺由来の細胞が存在していた事に疑いは無い。
内尿道括約筋(図中上側)は完全切除されるので、下側(外尿道括約筋)の細胞が残存している可能性はあるとおもわれる。前立腺由来の細胞はテストステロンの依存性があり、また上皮細胞であることから(テストステロンは前立腺のリダクターゼによりジハイドロテストステロンに合成される)前立腺細胞の再生を否定する事はできないが、PSA漏出での基底膜との関係が不明である。(最終章のPSA~参照)
癌細胞の好発部位は周辺部(前立腺下部)なので、癌細胞残存の可能性(浸潤転移不能のオリゴメタを含め)は当然排除出来ないが、PSA再発でのPSA100で臨床癌でないのはどうにも説明がつかない。血中PSAが上昇するには多巣性であれ、それなりの固形的な細胞形成が必要と思われるのだが・・・。 もしがん細胞が残るとすれば局所周辺微小環境(毛細血管、静脈叢か?)しか考えられない。
前立腺がんガイドラインではPSAdtが90~180日以下ならば将来生命リスクの伴う転移が出現する可能性を示唆している。これは傷などでの細胞再生速度より遅くはあるが、通常細胞代謝に比べ遥かに活発ではないかとの認識である。細胞再生(分裂)のエンドポイントがどこにあるかは判らないが、癌細胞増殖は生命の死をエンドポイントとしている事だけは確実である。
神経温存の場合、PSAは0.5を上回らない様である。
『癌取扱規約』TNM分類では転移は遠隔転移とリンパ行(領域)転移の二つだけである。何れもチューブを介在しての転移で、近傍への癌細胞の集団移動や転移は想定されていない。
私はいつも思うのだが、播種の伴わない全摘の『取り残しの癌細胞』って一体何なのであろう?。PSAだけが上昇する再発をNCCNは全身播種と言うが、これは何なんだろう?前立腺がんで、びまん(diffuse:非上皮性)性転移てあるんだろうか?血管内被に血栓の様にがん細胞が付着しているんだろうか?
なんでTNMにカテゴリーされていないんだろう?
なんでTNMにカテゴリーされていないんだろう?
≪リンパ節転移とPLND:ハルステッドからセンチネル・リンパ説≫
領域転移としてはリンパ行性がある。通常末梢が上流で左鎖骨下静脈角(右静脈角は右上半身のリンパだけ)で胸管(静脈)と合流する地点が丁度河口にあたる。なので、骨盤内にある癌からの上半身リンパ転移は通常左側(腋窩リンパ節)である。
脈管途中で癌塊などでの圧障害があると逆行性となるが、順行性である場合、転移したリンパ節のその上流に癌病巣が無ければならない。つまりリンパ領域の決まった1ケ所のリンパ節(センチネル)に転移がなければそれ以外に転移している可能性は極めて低いと思われてきた。が・・・、骨盤内のリンパ動態では違うようだ・・・(何故骨転移か?参照)
否、話を原点に戻そう。このリンパ行性、即ち経路の解明こそ『癌治療』そのものの歴史と云っていい。病理学者ウイルヒョウ(Virchow 1850~)の古典的腫瘍論(方向性追次リンパ転移後血行説)から始まったハルステドの癌拡大リンパ節切除手術は1970年初頭のRCT(大規模無作為比較試験)まで継続され、その後1977年医師カバナスがセンチネル・リンパ節を発見、モートン&アレックスが同リンパ節を同定し,1980年フイッシャー(fisher)の『固形がん全身病説』の成立まで我々の身体は常に強い侵襲性を余儀なくされてきた。現在でもこの『固形癌局処病説』そして『固形癌全身病説』の結論は得るに至ってはいない。が、併し、フィシャーの功績は大きく、内視鏡手術やリンパ節郭清不要論の流れを加速させ、前立腺がん手術では現在、PSA10以下 グリソンスコアー6以下ならリンパ郭清は不要とされている。高リスク(リンパ節転移確率>2%)の場合拡大(領域リンパ)郭清処理ですが、閉鎖は必須のようです。
≪inaの思い≫
前立腺がん手術の多くで閉鎖リンパは切除されます。断端(surgcal margin :尖部や尿道)が陰性の場合安心してもいいのかと思います。尚、鼠径リンパ節に転移があった場合現在ではN1では無く、M1(遠隔転移)とされています。また余談ですが導管癌を混在した場合もGS8とされています。
 |
| 閉鎖動脈ー閉鎖リンパ節 |
 |
| 領域リンパ節 |
≪術後のPSAは再発の指針となりえるのか?≫
幾度も云いますが、PSA再発でホルモン既往の場合では、血清PSA値が20~30、或いは耐剤性から100に近い人が稀なくおられます。これらの人々には臨床的に『がん』はありません。
術前PSA20となれば転移を疑い、100なれば転移の可能性が高いにも関わらずにです。 Charles R. Pound氏等によれば「10年間で約70%の確率で臨床がんに至る」 Natural history of progression after PSA elevation following radical prostatectomy. としていますが、私には実感としてはありません。余談ですが、 この6年前(1993,May)に同氏等は(Serum PSA after anatomic radical prostatectomy. The Johns Hopkins experience after 10 years.)の
要約の中で長いPSA再発期間の癌を、或いは一向に出現しない癌を「occult local recurrence」(オカルト局所再発)と述べています。このジレンマが著名なPSA大規模コホート調査の動機であった様に思います。6年後の1999,Nov,の事でした。
PSA末梢血への漏出は基底膜の喪失を原因としていますが、炎症の場合は免疫応答で基底膜から破壊が発生するのでその理解は可能と思われます。癌では基底膜の喪失があった場合に結果的に癌細胞はあるが、喪失因子は『がん』との証拠はありません。がん疾患での基底膜の喪失のモデルは、癌前駆細胞(前立腺上皮内腫瘍=PIN)ではPSAの上昇がない事をその根拠としているだけです。事実、導管癌では2相性(基底細胞)を保持しているPINのケースは多くあります。
また、前立腺がんの由来は基底細胞(幹細胞?)であるとして(基底細胞が脱分化して癌化)、基底膜がそもそも喪失している。そもそも論とかですが、確証たるものはありません。なので、基底膜の喪失を「がん」とし、腫瘍性病変を上皮内新生物(PIN:上皮内がん)と呼称している。
この場合『前立腺肥大症=BPH』でのPSA上昇の説明が出来ません。内圧説や腔所喪失説がありますがPSAはかなりの高分子(34kDa)で物理的にも、また、例えMMP(蛋白分解酵素)を分泌させたとしても基底膜(t50~100nm)を容易に透過しないと思いますが・・・。
術後PSAの源流は癌細胞でしょうか?キャンサーボリュムとPSAの相関が不明ですが、血清でNSEやALPなどの癌関連マーカが異常値でなく、画像でも癌の証拠がない(NED)場合、プラットホームの存在もなく全身に癌細胞(遊走するためにEMTされた形質転換細胞?)が遊走している事になります。 血中癌細胞の半減期は2.4時間と云う事らしいので、PSA値を維持するならば1日当たり10回の細胞分裂を必要とします。
大変に考え難い動態ではないでしょうか?
前立腺癌,前立腺肥大、嚢胞病変部及び導管と前立腺液
(下図ではPSAとなっていますが正確には前立腺液です)
参考前立腺癌,前立腺肥大、嚢胞病変部及び導管と前立腺液
(下図ではPSAとなっていますが正確には前立腺液です)
 |
| 前立腺腺房ー導管構造 PSA |
≪オカルト(PSA局所再発)から転移死亡例はあったのか?≫
(ベースライン・リスク:放置をすれば・・・)
(ベースライン・リスク:放置をすれば・・・)
実在不明なPSA局所再発のがんを「オカルト」 (occult local recurrence)と呼んだCharles R. Pound,達は1997人をリクルートした6年後のスタディ Natural History では、正体が隠れた「ハーバー」(harbor distant metastatic disease 潜在的遠隔転移がん) と述べている。
Natural History は前立腺がん根治手術後から遠隔転移するまでの自然放置した時間経路の調査である。このコホートの死亡因子は全て癌に起因するもので、それ以外の理由で死亡したものは誰もいない。PSA再発は304人、PSA再発後の遠隔転移は103人(保険数理で中央値8年)、転移後の死亡は44人(保険数理で中央値5年弱)。手術後15年間のレンジでのレトロスペクティブ(後ろ向き追跡調査:過去の洗い出し)である。
当然死亡起因は遠隔転移にあるが、遠隔転移に局所床(prostatic bed)が介在した可能性は言及されていない。つまり、局所再発して成長した癌が遠隔転移したのか、もしくは手術前に既に遠隔転移していたのか(オリゴメタ)、或いは転移経路(御旅所みたいなもの、微小がん転移元)としていたのかは、この分脈からは不明である。リテラシが無いと云われれば笑うしかないが、PSA再発した304人中83名は術後PSA値が高く放射線補助治療をうけたがPSA低下がなく遠隔転移とカテゴリされた。期間中の死亡者は103名、遠隔転移での死亡者が44名と云う事実に従うと、最大20名が局所再発からの転移であった可能性は否定できない。
だが、1997人、15年間で臨床的に局所(直腸、膀胱や尿道を含め)再発と記録された症例は1名たりとて存在しない。1次転移巣と2次転移巣との腫瘍形成のダブリングタイムが同じと言った説に従うならば、このスタディで遠隔転移と臨床診断されたその時点でオカルト局所再発は否定された事になる。少なくとも遠隔転移の経路では有り得ない。このスタディではT3b(手術推奨外:精嚢浸潤)が105名、リンパ転移(N1:D1)120名が患者登録されていた。
これは、勇気ある発言をするならば、PSA局所再発など実在しない事を意味している。僕は進行した局所再発の証拠(写真)を未だに見たことが無い。或いは、解剖において形態学的(目で解る)な癌組織の観察がされた事例も知らない。転移先でのみ増殖進行する癌細胞って存在するのだろうか?
PSAに注目すれば、この臨床試験の資格条件に満たず排除された人を含めるとPSA再発は315人(16%弱)だが、PSA上昇した人は術後5年で27%、10年で53%であった。このPSA再発率の低さは、リクルートした患者の術前ステージでT2c以上の人が151人、PSA20以上で96人(多数が10以下)、グリソンスコアーでは8-10の患者が155人という全てに於いて低リスクの好条件下であった所為かも知れない。
《リンパ行性と血行転移 何故骨転移か?(転移防止の裏技!! 立寝!!)》
TNM分類では血行性転移とリンパ行性転移の二分類とされ、リンパ行性からは膀胱に、或いは仙骨への転移が希に観察される。が、これらは直接侵蝕或いは逆流による転移であり、肺への転移もリンパ行性と云われているが血行性転移が普通である。リンパは領域転移とされている様に転移したリンパ節の、そのリンパ領域の臓器(骨を含む)に直接か逆流浸潤して転移されるのがリンパ行性である。
骨への転移は、漿膜の無い食道のがん等にみられる様な癌病巣から直接骨への侵蝕性転移はなく、静脈叢からの転移経路が多い。分類的には血行性骨転移である。複雑にしているのは静脈叢(傍椎体静脈)とリンパ管とは相互に交通していて、また骨盤及び脊椎静脈叢には弁構造がなく(硬膜外batson静脈)胸部、腹部、骨盤、脳と静脈還流系へ直接接続されていて血流も双方向性をとる為にがん細胞は複雑な転移形態をとると思われる。つまり、下大静脈を介さずに前立腺静脈叢と脊椎静脈叢は方向性なく接続されていて血液は湖のような溜まりをみせる。なので、脊椎や骨盤の転移、そしてtight junction機構を持つ脳関門の制限を得ない脳転移が容易に生じる。
venous lake(静脈湖)様と呼ばれるこれらの血液の淀みに漂うがん細胞は、或いはNCCNの言う全身播種を示唆するのかも知れない。
骨への転移は、漿膜の無い食道のがん等にみられる様な癌病巣から直接骨への侵蝕性転移はなく、静脈叢からの転移経路が多い。分類的には血行性骨転移である。複雑にしているのは静脈叢(傍椎体静脈)とリンパ管とは相互に交通していて、また骨盤及び脊椎静脈叢には弁構造がなく(硬膜外batson静脈)胸部、腹部、骨盤、脳と静脈還流系へ直接接続されていて血流も双方向性をとる為にがん細胞は複雑な転移形態をとると思われる。つまり、下大静脈を介さずに前立腺静脈叢と脊椎静脈叢は方向性なく接続されていて血液は湖のような溜まりをみせる。なので、脊椎や骨盤の転移、そしてtight junction機構を持つ脳関門の制限を得ない脳転移が容易に生じる。
venous lake(静脈湖)様と呼ばれるこれらの血液の淀みに漂うがん細胞は、或いはNCCNの言う全身播種を示唆するのかも知れない。
骨髄で造血された未成熟な血液細胞達は分裂を繰り返す度に分化され熟成した血液に成長していく。この静脈湖はウィスキーを寝かす樽と言えるかも知れない。
リンパ節による転移は直接臓器への接触浸潤であり、前立腺がんの場合の血行性骨転移では、大腸がんの肝転移(門脈経路系)と同様に、脊椎静脈系(basivertebral vein)の転移が多くみられ、肺転移や手足の抹消骨転移に多い循環系でない。
《骨転移部位(骨ストラクチュアー)》
では、骨のどこに転移するのか?何時するのか!!?
その前に骨のストラクチュアーから云います。一番外側に「外骨膜」があり2層目の「骨質(緻密骨:皮質骨)」と強力に接着され、3層目に「内骨膜」そして「海棉骨(骨梁間には骨髄)」最後に「骨腔」があり、黄色(成長期、短骨では造血球で赤色)の「骨髄」が充填されているイメージです。図C
皮質骨は丁度ロールケーキを収層構造したイメージで、一本のロールケーキをosteon、中心にhavers管(血管)、神経、リンパ、横断ではvolkmann管とでNETWORK網が敷かれています。図b
がん細胞は外部静脈管から骨へ浸潤侵入し、三つの分岐された血管に侵入しますと、血流の一番多い骨髄方向にがん細胞は分布される傾向があり、更にhavers管から分岐されたvolkmannで拡散されて海棉骨や骨髄に着床すると云われています。がん細胞は骨髄毛細血管で増殖すると言われています。もし、骨髄に浸潤すると汎血球減少症を合併し致死率は高くなります。肺がんからのパスウェイは動脈(栄養血管)となりますが四躯骨への転移は少ないようです。図C
転移を有した患者の86%弱が骨への転移です。経路は脳転移と同様batson静脈叢(傍推体静脈叢)と考えられ、最初に骨盤静脈叢から骨盤骨に転移し次に骨盤骨から肝臓へ転移し(多分、batson→門脈→肝臓だが、門脈も無弁なので何故消化器に転移しないのかは不明。解れば追記します。肺はbatsonと交通があります。)、3番目にはその上部に位置した肺へ、そして最後は脳へと、がん細胞は駆け昇ってきます。肝や肺に転移が無く脳に転移があった場合は肺循環経路では無く、batson経路の可能性が高い。
もし、がん細胞が肝静脈に流入した場合は肺転移は勿論、全身転移のリスクも高くなりそうです。
リンパ節と骨の転移順序はありません。
転移は複雑な経路を経て癌が昇りますが、上るほど疲れて(肝肺でのフイルター)転移頻度は下がると言われています。 リンパ節と骨の転移順序はありません。
《 転移の動態 ( がんは身体を駆け登る )日本人での調査 》
転移を有した患者の86%弱が骨への転移です。経路は脳転移と同様batson静脈叢(傍推体静脈叢)と考えられ、最初に骨盤静脈叢から骨盤骨に転移し次に骨盤骨から肝臓へ転移し(多分、batson→門脈→肝臓だが、門脈も無弁なので何故消化器に転移しないのかは不明。解れば追記します。肺はbatsonと交通があります。)、3番目にはその上部に位置した肺へ、そして最後は脳へと、がん細胞は駆け昇ってきます。肝や肺に転移が無く脳に転移があった場合は肺循環経路では無く、batson経路の可能性が高い。
もし、がん細胞が肝静脈に流入した場合は肺転移は勿論、全身転移のリスクも高くなりそうです。
リンパ節と骨の転移順序はありません。
転移は複雑な経路を経て癌が昇りますが、上るほど疲れて(肝肺でのフイルター)転移頻度は下がると言われています。 リンパ節と骨の転移順序はありません。
深夜のリンパ管挙動の静止や自律神経、血流の動態(臥位で前立腺静脈叢から骨盤骨へ流れ、立位では逆流:がん細胞も菌感染も同じ、また筋肉弛緩による静脈血の鬱滞はがん細胞の転移、接着を容易にし:がん細胞も血栓も同じ)もそうですが「生命のリズム(月の満ち千き)」がその理由です。何故「月」なのか?臓器の殆どの漢字は女性名詞の代表格である「月」に修飾されていて・・・ これ以上言うとバカにされそうなので、これで止めます。 失礼しました。・・・・ /m(- -)m しかし、ビカルタミド(カソデックス)の最大血中濃度は何時に設計されているかご存知ですかぁ~・・・・次行きます。
《骨転移予防と虫歯予防ついでにリユウマチ》
病理学的分類では前立腺がんは乳がんや肺がんとは異なり胃がんに多い造骨型(骨形成)となりますが、組織学的には溶骨混在型となります。がん細胞が周辺の間葉質系細胞(骨芽細胞、コラーゲン)を刺激して、或いはマクロファージが、PGE2(プロスタグランジンE)を放出させ、ナイーブTho細胞をTh2細胞(液性)に分化させ、骨髄由来のマクロファージ未成熟単球細胞を多核細胞である破骨細胞に分化・融合させていきます。ここら辺は虫歯と同じプロセスを辿ります。尤も虫歯の場合はミュータンスによる乳酸産生と歯髄が関与しますが・・・。以前アレルギー性体質は転移し易い(癌:真菌説を追うⅠ)で書きましたが、リユウマチを含め元凶はアラキドン酸だと思います。マルで余談ですが・・・癌真菌説では癌はカンジタ菌であるとイタリアのMD(メディカル・ドクター)は言いましたが、カビキラーで癌は改善しません。同様に骨転移にライオンやサンスターは何の役にもたちません。役にたつのは成分にあるハイドロキシアパタイトぐらいでしょうか。
では、どうするか?骨組織に侵入したがん細胞は間質細胞やマクロファージからIL1βやIL6(インターロイキン:破骨洰胞活性化因子)PGE2を発現させ正帰還的に破骨細胞を活性化させる。これらのサイトカインはリュウマチ患者にも多く発現(関節液)しており、骨吸収を亢進させ骨萎縮を誘導する。破骨細胞の抑制にはゾレドロン酸(ゾメタ):ビスホスホネートが使用されているが、既に報道されている様に今後に向けて顎骨壊死する人が増加する可能性も否定できない。
立ち寝もできない我々はどうするのか?傾斜型ベッドにすればがん細胞は頭に上がれないかも知れない。タダで出来る対策は効果なし?そんな事はありません。あのエコノミー症候群(long flight 深部静脈血栓症)でも時偶足を上げて寝るだけで一命が助かるんですから。血の流れをバカにしてはあきません。しかし、根本的な対策ではない。転移防止用ベッドでも開発されれば話は別だが・・・。
立ち寝もできない我々はどうするのか?傾斜型ベッドにすればがん細胞は頭に上がれないかも知れない。タダで出来る対策は効果なし?そんな事はありません。あのエコノミー症候群(long flight 深部静脈血栓症)でも時偶足を上げて寝るだけで一命が助かるんですから。血の流れをバカにしてはあきません。しかし、根本的な対策ではない。転移防止用ベッドでも開発されれば話は別だが・・・。
そもそも、がんも老化も酸化(酸素結合:水素放出(イオンではない)電気的には電子が流れていく・ポテンシャルの喪失)が原因である。放射線治療も抗がん剤もこの原理である。細胞と酸化還元(レドックス制御)・脂質と膜は次に行きたいと思いますが、骨転移の予防はアレルギー対策と同じで、リノール酸、アラキドン酸(PGE2)を控え味噌やヨーグルト、納豆等或いはアスピリン、ジキニンやイブ(イブプロフェン)を摂取すればIL-6を抑制し酸化し易い体質が改善されるかもしれない。これは前立腺がんだけでなく、乳がんや結腸がん細胞の増殖をも阻害すると言われている。
前立腺癌患者の約半数に悪液質(カヘキシー)があると言う。IL6を抑制すれば改善する。(kuroda et al, urology 69,2007)
ウソぽい話だが、リュウマチ患者には重篤なガン患者が少ないと言われている。抗炎症剤セレブレックス(セレコックス:selecoxib)服用が理由と考える論文もあります。
飲み薬はど~かな~と言う人には股間や下腹部にエアーサロンパス、アンメルシンヨコヨコ、パテックス、バンテリン等を貼り付けたり塗ったりするとインドメタシンの作用で前立腺がん再発予防に効果的かも知れない( 僕はしていませんが・・・)。
夜間頻尿にはロキソニンやセレコックスが処方されると言う。
過度の性行為、特に射精痛などがあるとPGE2が多量に産生誘起され転移や憎悪の原因になる可能性があるので控えたほうがいいのかも知れない。
《 発癌性が強力なほど効果的な抗がん剤と放射線治療。そしてレドックス。》
《がんの因子》
《体細胞の生と死》
《修復遺伝子と自殺遺伝子、そして免疫での非自己-食殺》
《放射線と抗がん剤 そしてレドックスへ》
前立腺癌患者の約半数に悪液質(カヘキシー)があると言う。IL6を抑制すれば改善する。(kuroda et al, urology 69,2007)
ウソぽい話だが、リュウマチ患者には重篤なガン患者が少ないと言われている。抗炎症剤セレブレックス(セレコックス:selecoxib)服用が理由と考える論文もあります。
飲み薬はど~かな~と言う人には股間や下腹部にエアーサロンパス、アンメルシンヨコヨコ、パテックス、バンテリン等を貼り付けたり塗ったりするとインドメタシンの作用で前立腺がん再発予防に効果的かも知れない( 僕はしていませんが・・・)。
夜間頻尿にはロキソニンやセレコックスが処方されると言う。
過度の性行為、特に射精痛などがあるとPGE2が多量に産生誘起され転移や憎悪の原因になる可能性があるので控えたほうがいいのかも知れない。
《 発癌性が強力なほど効果的な抗がん剤と放射線治療。そしてレドックス。》
《がんの因子》
《体細胞の生と死》
《修復遺伝子と自殺遺伝子、そして免疫での非自己-食殺》
《放射線と抗がん剤 そしてレドックスへ》
Notes
使用しているイラスト(図)はNETからオリジナルを借用して加工しています。著作権等の問題がありましたらばご連絡ください。即時消去します。ina.takasi@gmail.com
その前に、この素晴らしき作者達に深い敬意を表します。
その前に、この素晴らしき作者達に深い敬意を表します。
ダブリングタイム(倍加時間):腫瘍体容積(細胞数)が2倍になる時間。転移先によりがん細胞は変質するが、母細胞の倍加時間は転移先でも原則同一とする説(EMT-MET)や、転移先に依存する説、色々いわれている様ですが、転移能がある細胞質だけが転移するので一般的にダブリングタイムも早いと思っています。なので、原発巣よりも転移巣の成長ははやいと思っていますが、薬剤やガンマーカーの応答性の違いはあるが、増殖率は同じと言った報告もあり、僕は正直あまり良く分かりません。前立腺がんで言えば原発巣、転移巣、1次転移、2次転移等のダブリングタイムは同じではないかと思っています。転移先でも均一の細胞組織の形成は出来ないだろうと想像してるのが理由です。
乳がんでは原発巣DT平均96日⇒肺転移病巣DT平均74日となっています。
EMT(Epithelial-Mesenchymal transition:上皮間葉転換)はがん細胞が転移する時に上皮分化形質から間葉系様細胞に表現を変え血管内を遊走します。 MET: (Mesenchymal-Epithelial transition:間葉上皮転換) は血管内で遊走していたがん細胞が新たな転移場所でMMP(タンパク質分解酵素)などを分泌して血管を溶解脱出して他臓器に接着する時に元の細胞質(上皮細胞由来)にリモデリングします。新たな転移メカニズムの仮説ですが、前立腺がん転移の場合では低分化がんでは血管浸潤でEMT変換しますが、高分化型では細胞単体ではなく血管内皮に包囲されたクラスター(非浸潤型:癌胞巣=団子)転移ではないかと思っています。
転移先がパッシブ(消極的受け入れ)なのか、或いはアクティブ(積極的誘導)なのか結論は得ていませんが現時点では誘地論が優勢な様です。ここでの問題はPSAですが、前立腺がん細胞が接着分子から離脱するためにもしも間葉系細胞(stroma)に細胞変身した場合のPSA値の変化については、残念ながら僕にはわかりません。
乳がんでは原発巣DT平均96日⇒肺転移病巣DT平均74日となっています。
EMT(Epithelial-Mesenchymal transition:上皮間葉転換)はがん細胞が転移する時に上皮分化形質から間葉系様細胞に表現を変え血管内を遊走します。 MET: (Mesenchymal-Epithelial transition:間葉上皮転換) は血管内で遊走していたがん細胞が新たな転移場所でMMP(タンパク質分解酵素)などを分泌して血管を溶解脱出して他臓器に接着する時に元の細胞質(上皮細胞由来)にリモデリングします。新たな転移メカニズムの仮説ですが、前立腺がん転移の場合では低分化がんでは血管浸潤でEMT変換しますが、高分化型では細胞単体ではなく血管内皮に包囲されたクラスター(非浸潤型:癌胞巣=団子)転移ではないかと思っています。
転移先がパッシブ(消極的受け入れ)なのか、或いはアクティブ(積極的誘導)なのか結論は得ていませんが現時点では誘地論が優勢な様です。ここでの問題はPSAですが、前立腺がん細胞が接着分子から離脱するためにもしも間葉系細胞(stroma)に細胞変身した場合のPSA値の変化については、残念ながら僕にはわかりません。
血小板系細胞は分裂を伴わない分化形式のようです。
参考文献













0 件のコメント:
コメントを投稿